专注于为全球制药企业和生物技术公司提供全面的生物分析服务,致力于打造符合国际标准的分析检测技术平台,质量体系遵循NMPA、EMA、FDA和ICH等法规要求,是一家专业高效地提供一站式临床生物分析服务的实验室。
已在南北两地(北京首研和杭州安渡)成功运营2个符合GLP标准的生物分析实验室。我们的技术团队由专业背景深厚的人员组成,拥有丰富的方法学开发、验证、样本分析、注册申报及项目管理等全流程服务经验,可提供支持疫苗及各类药物和疗法,包括小分子化药、蛋白/多肽、单抗及多特异抗体、偶联药物(XDC)、小核酸、细胞和基因治疗等。同时提供非临床和临床开发的PKPD分析、免疫原性评估和生物标志物检测等服务。

疫苗分析
提供全面合规,且支持各类疫苗临床研究的生物分析服务,已开发和验证诸多分析方法,亦可定制开发
疫苗类型:肺炎球菌/脑膜炎球菌/人乳头瘤病毒/带状疱疹/呼吸道合胞病毒/流感/诺如病毒等
疫苗类型:肺炎球菌/脑膜炎球菌/人乳头瘤病毒/带状疱疹/呼吸道合胞病毒/流感/诺如病毒等

LC-MS/MS
利用高分辨和三重四级杆质谱测定抗体偶联药物(ADC)、寡核苷酸、肽、小分子和生物标志物、PROTAC等

PK、PD分析
深入理解生物学和靶点,开发多种生物技术药类型的分析方法,支持生物技术药的非临床和临床研究,帮助申办方了解药物在体内作用的物质基础

免疫原性
利用多重和超灵敏ELISA、MSD、Gyrolab、Luminex和SPX进行蛋白质/寡核苷酸疗法、生物标志物和抗药物抗体分析
生物标志物
在炎症因子、趋化因子、血管内皮生长因子等生物标志物检测方面拥有丰富的经验
已建成蛋白和细胞的生物标志物分析平台,可实现高灵敏度和高特异性的多指标分析,助力申办方进行生物标志物探索
已建成蛋白和细胞的生物标志物分析平台,可实现高灵敏度和高特异性的多指标分析,助力申办方进行生物标志物探索

生物样本管理
通过Watson LIMS进行生物样本全生命周期管理,支持各类生物样本从采集、运输、接收、储存、使用和处置的规范性,可全程审计追踪,确保样本安全

定制化的分析方法开发
团队拥有丰富的方法开发经验,尤其是针对新的技术平台,积累了针对新分子类型的分析方法开发能力,可以快速跟进生物药领域不断涌现的需求
我们的实验室拥有尖端的技术和一流的设备,支持新方法开发和验证
我们的实验室拥有尖端的技术和一流的设备,支持新方法开发和验证

广泛的专业知识和全面的技术经验
凭借团队在药物开发方面广泛的专业知识和全面的技术经验,可操作复杂方法转移或分析方法开发,并生成报告,为临床前和临床开发阶段定制样本分析方案
团队的核心人员拥有多年创新药研发经验,可从药物研发全流程角度,在药物研发的不同阶段,为项目制定针对性的生物分析策略
团队的核心人员拥有多年创新药研发经验,可从药物研发全流程角度,在药物研发的不同阶段,为项目制定针对性的生物分析策略

全面的免疫原性评估可支持新药入市申报
实验室免疫原性评价体系完善,具备体液免疫、细胞免疫及病原微生物实验检测技术。我们全面的解决方案包括:
免疫原性风险评估和临床免疫原性策略
检测方法开发和验证
样本检测(抗药抗体筛选、确认、滴定、中和能力、表位特异性、同种异体)
临床开发中的数据分析(抗药抗体对药代动力学/药效学的影响、疗效和不良反应)
法规申报文件(如免疫原性的综合摘要,2.7.1,2.7.2、CSR等)
免疫原性风险评估和临床免疫原性策略
检测方法开发和验证
样本检测(抗药抗体筛选、确认、滴定、中和能力、表位特异性、同种异体)
临床开发中的数据分析(抗药抗体对药代动力学/药效学的影响、疗效和不良反应)
法规申报文件(如免疫原性的综合摘要,2.7.1,2.7.2、CSR等)

助力临床开发一体化
依托于斯丹姆集团近20年丰富的临床开发服务经验,提供一站式药物临床开发服务,提高沟通和协同效率,可极大保障项目执行和交付质量,高效推进项目进程,助力产品商业化
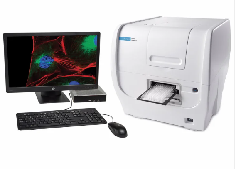
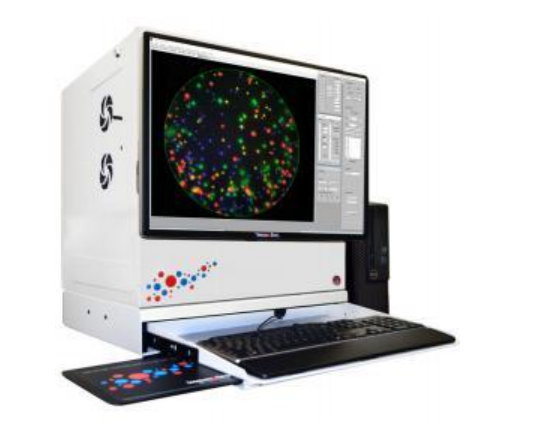
主要仪器设备